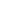
Quy chế về y tế thay đổi thường xuyên và những thay đổi này có thể có tác động đến việc đăng ký sản phẩm của bạn với các nhà quản lý trong và ngoài nước.
Chúng tôi có một đội ngũ các chuyên gia để hỗ trợ các nhà sản xuất thiết bị y tế nhằm gia nhập thị trường một cách nhanh chóng và tiếp tục tuân thủ các quy định mới nhất trong những thị trường chủ lực.
STC có thể hỗ trợ việc toàn bộ quá trình đăng ký thuốc từ phân loại sản phẩm – phân tích khoảng trống giá - tìm nguồn cung ứng các thành phần y tế - soạn tập tin / hồ sơ kỹ thuật - kiểm tra theo tài sản thế chấp, đặc biệt là các tiêu chuẩn hài hoà và / hoặc tiêu chuẩn công nghiệp – thiết lập thiết bị thử nghiệm để thử nghiệm hiệu suất - Thử nghiệm sinh học theo yêu cầu GLP - nộp hồ sơ kỹ thuật các nhà hành pháp - đại diện tại địa phương – Sở hữu giấy phép- Quản lý rủi ro – hỗ trơ tại chỗ khi có thanh tra kiểm định.
Cơ sở thử nghiệm sinh học GLP của chúng tôi nằm ở Đông Quan hỗ trợ thử nghiệm ISO10993 theo yêu cầu chế định.
Thử nghiệm bao gồm:
- Thử nghiệm tương tác với máu [ISO10993-4]
- Vitro độc tế bào [ISO 10993-5]
- Hiệu ứng bộ phận sau khi cấy ghép [ISO 10993-6]
- Lượng dư chất khử trùng Ethylene oxide [ISO10993-7]
- Kích thích [ISO 10993-10]
- Độ mẫn cảm của da [ISO 10993-10]
- Hệ thống độc tính [ISO10993-11]
Thử nghiệm hỗ trợ theo nhóm tiêu chuẩn IEC60601 bao gồm EMC, an toàn và hiệu suất điện năng.
QMS / QSR hỗ trợ cho CFR820, ISO13485, MDR Canada, GMP Hàn Quốc, GMP Brazil, Pháp lệnh 169 Nhật Bản.
Chúng tôi hỗ trợ thị trường trọng điểm FDA Mỹ, HC Canada, MDD cơ quan thông báo CE, NMPA Trung Quốc, TFDA Đài Loan, MFDS Hàn Quốc, MHLW Nhật Bản, Bộ Y tế Malaysia, HAS Singapore, Bộ Y tế Ấn Độ, Sở Y tế Úc, và Bộ Y tế Brazil.
Để biết thêm thông tin về dịch vụ thử nghiệm, vui lòng Liên hệ với chúng tôi















